Разделы сайта
В чем сущность установления химического равновесия? Графики изменения скорости прямой и обратной реакции
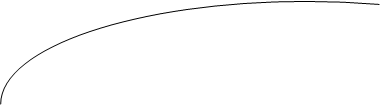
На рисунке 2 показано изменение скоростей прямой и обратной реакции с течением времени. В начале, при смещении исходных веществ, скорость прямой реакции велика, а скорость обратной реакции равно нулю. По мере протекания реакции исходные вещества расходуются и их концентрации падают. В результате этого уменьшается скорость прямой реакции. Одновременно появляются продукты реакции, и их концентрация возрастает. Вследствие этого начинает идти обратная реакция, причем ее скорость постепенно увеличивается. Когда скорости прямой и обратной реакций становятся одинаковыми, наступает химическое равновесие.
Рис. 2. Изменение скорости прямой (v1) и обратной (v2) реакций с течением времени (t).
![]()
 v
v
v1
 v1=v2
v1=v2
v2
t
Химическое равновесие называют динамическим равновесием
. Этим подчеркивается, что при равновесии протекают и прямая, и обратная реакции, но их скорости одинаковы, вследствие чего изменений в системе не заметно.
Количественной характеристикой химического равновесия служит величина, называемая, константой химического равновесия.
Отношение констант скорости прямой и обратной реакций, тоже представляет собой константу. Она называется константой равновесия данной реакции (K): k
1/
k
2=
K
.
Отсюда окончательно: [
HI
]²/ [
H
2] [
I
2]=
K
.
В левой части этого уравнения стоят те концентрации взаимодействующих веществ, которые устанавливаются при равновесии – равновесные концентрации. Правая же часть уравнения представляет собой постоянную (при постоянной температуре) величину.


